Abstrakt
K predĺženiu života pacientov s nádorovým ochorením prispieva aj možnosť podávania parenterálnej výživy (PV) v prípadoch zlyhania tráviaceho traktu. Napriek tomu indikácia PV zostáva kontroverznou témou hlavne u paliatívnych pacientov, pretože nemáme definované prediktory benefitu v tejto nehomogénnej skupine pacientov.(1) 1. 1. 2015 vzniklo Centrum DPV pri Národnom onkologickom ústave v Bratislave. Do programu nášho centra sme do 31. 12. 2018 zaradili 89 pacientov. Z toho bolo 67 (75,3 %) pacientov s pokročilým nádorovým ochorením a 12 (24,7 %) pacientov s vyliečeným nádorovým ochorením. Priemerná dĺžka podávania PV u paliatívnych pacientov je 4,7 mesiaca a u vyliečených 33 mesiacov. Medián podávania PV je u paliatívnych pacientov 3 mesiace a u vyliečených 33 mesiacov. V súbore sme hodnotili aj tzv. biochemické nutričné parametre a naše výsledky sme porovnali s dokumentovanou literatúrou.
Kľúčové slová: domáca parenterálna výživa, pokročilé nádorové ochorenie, paliatívna medicína
Abstract
Access to the home parenteral nutrition (HPN) program among the patients with cancer could provide a survival benefit in case of gastrointestinal tract dysfunction. Hovewer indication of parenteral nutrition remains a controversal issue mainly among the patients with advanced cancer because there is no clear predictors of benefit (1). The HPN Centre in National Oncology Institute in Bratislava has provide HPN program for 89 patients untill 31.12.2018. Patients with advanced cancer and cancer survivors represent 67 (75,3%) and 12 (24,7%) respectively. Mean duration of HPN in advanced cancer patients and cancer survivors is 4,7 months and 33 months respectively. Median duration of HPN in advanced cancer patients and cancer survivors is 3 months and 33 months respectively. In the sample of patients we evaluated some biochemical nutritonal parametres. We compared our results with documented literature results.
Key words: home parenteral nutrition, advanced cancer, palliative medicine
Úvod
Vďaka skvelým pokrokom v medicíne za posledné roky sa znižuje úmrtnosť na nádorové ochorenia. Pacienti s pokročilým nádorovým ochorením žijú dlhšie. K predĺženiu života prispieva aj možnosť podávania parenterálnej výživy (PV) v prípadoch zlyhania tráviaceho traktu.
Indikácia parenterálnej výživy (PV) zostáva kontroverznou témou hlavne u paliatívnych pacientov. V štúdii profesora Bozzettiho z roku 2014, do ktorej bolo zahrnutých 414 pacientov s nevyliečiteľným nádorovým ochorením a obštrukciou gastrointestinálneho traktu rôzneho stupňa, sa zisťovalo, či existuje charakteristika, ktorá priamo súvisí s prežívaním kachektických pacientov pri podávanej PV. Skúmal sa vzťah medzi prežívaním a demografickými údajmi, nutričným stavom (BMI, úbytok hmotnosti), klinicko-onkologickým zhodnotením (Karnofského prognostické skóre (KPS), prognostikácia, primárny nádor, histológia, postihnutie životne dôležitých orgánov, staging, biochemické ukazovatele, trvanie domácej parenterálnej výživy (DPV)). Do štúdie bolo zapojených 13 centier z 10 krajín a štúdia trvala 6 rokov. Na základe multivariantnej analýzy s prežívaním najviac súviselo takzvané Glasgowské prognostické skóre (GPS). Pacienti, ktorí najdlhšie profitovali z podávanej parenterálnej výživy, mali GPS 0, čiže mali normálne hladiny albumínu a prozápalová aktivita vyjadrená eleváciou CRP nebola prítomná.(2)
Kazuistika
1. 1. 2015 vzniklo centrum DPV v Národnom onkologickom ústave v Bratislave. Vzniklo z potreby a začínajúcej praxe, ktorá sa začala realizovať u pacientov so syndrómom krátkeho čreva po opakovaných resekciách pre nádorové ochorenie a u pacientov so syndrómom malígnej črevnej obštrukcie, kde postihnutie čreva tak znižovalo zabezpečenie energetických potrieb, že by pacienti skôr umierali na vyhladovanie ako na progresiu nádorového ochorenia. Jedna pacientka z obdobia spred roka 2015 žije doteraz, v programe DPV je od júna 2010. Typickou pacientkou z väčšej skupiny pacientov s malígnou črevnou obštrukciou bola napríklad pacientka, ktorej bol ako 48-ročnej diagnostikovaný adenokarcinóm colon ascendens, iniciálne IV. klinické štádium s infiltráciou do brušnej steny a peritonea. V decembri 2013 jej bola realizovaná pravostranná hemikolektómia s histologicky potvrdenou infiltráciou peritonea. Do roka, v októbri 2014, bola realizovaná pre recidívu ochorenia v zmysle infiltrácie adnex, ovárií, uteru a znova lokalizovanej karcinomatózy peritonea hysterektómia, adnexektómia a resekcia sigmy s Dixonovou anastomózou. O pol roka, v máji, bola verifikovaná progresia ochorenia s chirurgicky neriešiteľným ileóznym stavom, s nutnosťou dekompresie nazogastrickou sondou. Z chirurgickej kliniky bola preložená na paliatívne oddelenie. Pri komplexnej antisekrečnej, antiemetickej a analgetickej liečbe sa podarilo odstrániť nazogastrickú sondu a pri podávaní parenterálnej výživy a hydratácie na oddelení sa začal stav výkonnosti pacientky zlepšovať. Od júna 2015 bola v programe DPV, pričom do októbra 2016 dostala dve línie systémovej protinádorovej liečby. Pacientka s podporou DPV prežívala 17 mesiacov, pričom DPV trvala 11 mesiacov. Pri podávanej chemoterapii sa podarilo obnoviť funkčnosť tráviaceho traktu a pacientka mohla mať perorálny príjem. Naopak, pri progresii ochorenia v závere života bola prítomná anasarka, ktorá bola znamením refraktérneho katabolizmu. Posledný mesiac pacientkinho života bol program DPV ukončený a pacientka zomierala s adekvátnou hydratáciou a komplexnou konzervatívnou liečbou malígnej črevnej obštrukcie vrátane paliatívnej sedatívnej liečby v samom závere života.
U pacientov s pokročilým nádorovým ochorením treba medicínsky definovať úskalia (komplikácie DPV) a limity (refraktérny katabolizmus, neschopnosť anabolizmu pri pokročilom nádorovom ochorení). Je potrebné zadefinovať ich pri indikácii, ale aj odkomunikovať pacientovi pri zaradení do programu DPV. O zmysluplnosti podávania parenterálnej výživy pacientom s pokročilým nádorovým ochorením treba diskutovať so samotným pacientom, ktorý by mal byť na začiatku informovaný o charaktere svojho nádorového ochorenia a o tom, že benefit parenterálnej výživy bude dočasný. V klinickej praxi sme mali prípady, keď pacient po oboznámení sa so svojím stavom odmietol DPV.
Zaraďovanie do programu DPV
zahŕňa zabezpečenie centrálneho venózneho prístupu, odsledovanie klinického benefitu počas hospitalizácie, zabezpečenie informovaného súhlasu, zaučenie pacienta. V priebehu programu DPV je nutné, aby pacient absolvoval pravidelné kontroly na prevenciu komplikácií a opakované hodnotenie benefitu parenterálnej výživy.
Edukačný program pre pacientov zaraďovaných do programu DPV musí zahŕňať starostlivosť o centrálny venózny katéter (CVK), pumpu alebo o iný systém dávkovania infúznej liečby, rozoznanie komplikácií a ich prevenciu. Poučenie musí vykonávať sestra zodpovedná za edukačný program v rámci centra. DPV je komplexná starostlivosť a výber pacientov vhodných do tohto terapeutického programu je kľúčovým aspektom dobrého výsledku. Pred zaradením do tréningového programu DPV je potrebné zhodnotiť pacientove kognitívne a fyzické schopnosti. Okrem medicínskych kritérií na zaradenie pacientov musíme zohľadniť aj rehabilitačný potenciál pacienta, sociálne a ekonomické faktory – niektoré aspekty starostlivosti v programe DPV vyplácané zdravotnou poisťovňou nie sú.
Na základe sociálnej nespôsobilosti alebo opakovaného porušenia dohodnutého protokolu je možné pacienta z programu DPV vyradiť, aj keby to malo znamenať pre neho fatálne následky. Túto situáciu sme riešili v praxi u pacienta po radikálnej operácii pre karcinóm pankreasu. Pacient mal ťažkú malnutríciu pre exokrinnú insuficienciu po totálnej duodenopankreatektómii s opakovanými hnačkami. Malnutrícia bola príčinou aj opuchového stavu. Po začatí parenterálnej výživy na oddelení sme pozorovali klinické zlepšenie a prírastok hmotnosti. Problém bol po prepustení pacienta domov. Po opakovanom nepriznaní kaválovej infekcie a neohlásení horúčky sme napriek poučeniu pacienta, dcéry a manželky urobili záznam do zdravotnej dokumentácie, pri ktorom sme zadefinovali problémy, pre ktoré sme ho z programu DPV vyradili: opakované neohlásenie horúčky pri zavedenom CVK.
Zistilo sa, že ak sa pri tréningu používajú písané manuály alebo videá a ak sa robí známkovanie pri každom tréningu, zlepšuje sa sebauvedomenie a zručnosť pacientov a rodinných príslušníkov pri manipulácii s prípravkami DPV. Kľúčom na poskytovanie efektívnej edukácie by mali byť definovaní členovia edukačného tímu DPV, nie všetky sestry na jednotlivom oddelení centra.(9)
Súbor zaradených pacientov – charakteristika
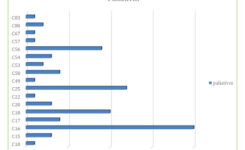
V našom centre sme zaradili do 31. 12. 2018 89 pacientov. Počet aktívnych pacientov v jednom mesiaci v programe DPV sa aktuálne pohybuje od 10 do 15. Zaraďovanie pacientov je znázornené v grafe č. 1.
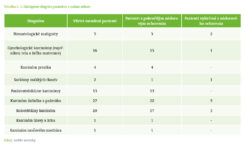
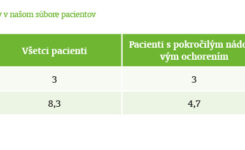
V tabuľke č. 1 sú počty zaradených pacientov podľa diagnóz. U paliatívnych pacientov je väčšinou príčinou zaradenia do programu DPV malígna črevná obštrukcia, ktorá je najčastejšie prítomná pri karcinóme vaječníkov a kolorektálnom karcinóme.(6) Zastúpenie diagnóz u našich paliatívnych pacientov je podobné ako v spomínanej literatúre a podrobne je znázornené v grafe č. 2. Priemerná dĺžka podávania PV u paliatívnych pacientov je 4,7 mesiaca a u vyliečených pacientov je to 33 mesiacov. Medián podávania PV je u paliatívnych pacientov 3 mesiace a u vyliečených 33 mesiacov. Tieto údaje sú zhrnuté v tabuľke č. 2. Z nášho súboru 89 pacientov bolo 67 (75,3 %) pacientov s pokročilým nádorovým ochorením. Zhodnotenie a stratifikácia pacientov podľa nutričných parametrov v našom súbore je zhrnutá v tabuľke č. 3. Väčšina pacientov zaradených do programu DPV (65,2 % zo všetkých zaradených pacientov) mala BMI nižšie ako 20. Viac ako polovica všetkých zaradených pacientov (57,3 %) mala normálnu cholínesterázu, 62,9 % zaradených pacientov malo zníženú hladinu prealbumínu a 68,5 % malo zníženú hladinu albumínu. Zo súboru paliatívnych pacientov (n = 67) sme PV podávali jeden mesiac u siedmich pacientov (10,3 %), 2 – 6 mesiacov trvalo podávanie PV u 36 pacientov (53,7 %) a viac ako 6 mesiacov dostávalo PV 6 paliatívnych pacientov (9 %).
Diskusia
Dĺžka trvania DPV je hlavne u pacientov s pokročilým nádorovým ochorením otázkou správnej prognostikácie. Problém je, že lekári často nadhodnocujú prognózu pacientov(7) a práve prognostikácia na základe Glasgowského prognostického skóre (GPS) pomáha zvládnuť túto často náročnú úlohu onkológa.(2) Prognostikácia môže byť aj na základe vývoja parametrov v čase, nie je to len statický údaj, preto je u pacientov relevantný terapeutický pokus, ktorým môžeme oddiferencovať refraktérnu kachexiu s neschopnosťou anabolizmu od tzv. anabolického okna, keď pacient môže utilizovať substráty PV aj pri prítomnosti generalizovaného nádorového ochorenia.(8, 10) V našom súbore pacientov s pokročilým nádorovým ochorením je medián podávania parenterálnej výživy porovnateľný s výsledkami multicentrickej štúdie prof. Bozzettiho F. a kolektívu, kde pacienti priemerne prežívali 4,7 mesiaca a medián prežívania s DPV bol 3 mesiace.(2)
V našom súbore nemáme zaznamenané celkové prežívanie, ale dĺžku trvania parenterálnej výživy. Oba údaje máme zhodné s prácou prof. Bozzettiho F. a kolektívu – priemerná dĺžka trvania programu DPV u pacientov s pokročilým nádorovým ochorením je 4,7 mesiaca a medián je 3 mesiace. Ako sme uviedli v kazuistike pacientky v úvode článku, v terminálnej fáze PV pacientom nepodávame. Všeobecne u pacientov s pokročilým nádorovým ochorením je vážnym problémom ukončenie parenterálnej výživy. Na konci života pri refraktérnom katabolizme(5) vyčerpaný organizmus neutilizuje substráty PV a aj adekvátny príjem parenterálnych tekutín spôsobuje pacientovi zhoršovanie jeho zomierania – zintenzívňovanie opuchového stavu, zvýraznenie terminálneho chrčania, zintenzívňovanie vracania pri malígnej črevnej obštrukcii.(3, 4) Z nášho súboru 89 pacientov bolo 67 (75,3 %) pacientov s pokročilým nádorovým ochorením. U siedmich pacientov zo spomínaných 67 paliatívnych, čo predstavuje 10,4 % z tejto skupiny, sme PV podávali len mesiac. U týchto pacientov bola prognostikácia zrejme nesprávna. PV u pacientov s nevyliečiteľným ochorením je pri indikácii a začatí v podstate terapeutickým pokusom, ktorý je relevantný, pretože neexistujú biomarkery, ktoré by vopred pacienta zadefinovali, či bude z PV profitovať, alebo nie.(4) Ak sa objavia komplikácie alebo nie je naplnený vopred stanovený terapeutický cieľ, pokus má byť ukončený.(4) Len 6 (9 %) pacientov zo skupiny 67 paliatívnych pacientov malo GPS 0, čo znamená, že pacientov s najlepšou prognózou profitovať z PV bolo najmenej v súbore. Prof. Bozzetti mal vo svojom súbore 16,6 % pacientov s GPS 0. Rovnako zastúpenie paliatívnych pacientov s GPS 1 v našom súbore bolo 47,5 verzus 28,4 % v súbore prof. Bozzettiho F. a kolektívu. V našom súbore bolo najviac pacientov s GPS 2 – 62,7 % paliatívnych pacientov.
Napriek tomu sú priemerná dĺžka trvania PV a medián trvania PV v našom súbore pacientov rovnaké ako v práci prof. Bozzettiho, hoci v jeho práci je referované prežívanie a v našom súbore ide o dĺžku podávania PV, pričom PV – ako som už spomenula – nepodávame do smrti. Je možné, že naši pacienti sú do programu DPV referovaní pomerne neskoro, čo súvisí s dostupnosťou paliatívnej starostlivosti na Slovensku, ale tiež to môže súvisieť s nízkym povedomím ošetrujúcich onkológov o benefite v zmysle predĺženia prežívania u pacientov s malígnou črevnou obštrukciou.
Záver
Centrum DPV pri Národnom onkologickom ústave má vo svojom súbore pacientov porovnateľné ukazovatele ako dostupné publikované dáta. DPV je relevantnou možnosťou na predĺženie individuálnej dĺžky života v prípade zlyhania funkčnosti tráviaceho traktu. Zrejme nie je všeobecne dostupnou na Slovensku.
MUDr. Andrea Škripeková, PhD.
II. onkologická klinika LF UK a NOÚ, Bratislava
E-mail: andrea.skripekova@nou.sk