Úvod
Začiatkom septembra 2017 sa konal v holandskom Haagu 39. ročník kongresu Európskej spoločnosti pre parenterálnu a enterálnu výživu. Paralelne prebiehalo niekoľko sekcií. Diskutovanou témou bola pretrvávajúca prevalencia iatrogénneho underfeedingu u kriticky chorých pacientov so zameraním sa na optimalizáciu výživy.(1) Na základe recentne publikovaných ESICM clinical practice guidelines sa kladie dôraz na začatie včasnej enterálnej výživy u väčšiny ICU (intensive care unit) pacientov, ktorí nemajú relatívnu ani absolútnu kontraindikáciu.(6) Bol prezentovaný nový pozmenený koncept vo výžive kriticky chorých pacientov: „more is better“ sa prehodnocuje podľa najnovších dát na „Baby stomach concept“ v analógii s „Baby lung“ teóriou u pacientov s ARDS.(5) Ďalšou zaujímavou témou bolo porovnanie lipidových emulzií a ich benefit na celkový outcome ICU pacientov.(9) Praktickou témou, s ktorou sa stretávame v každodennej praxi, bola dysfunkcia GITu z pohľadu pacienta. Odzneli praktické návody, ako postupovať pri meraní gastrického reziduálneho objemu. Vzhľadom na to, že súčasné európske odporúčania sú podľa najnovších poznatkov kontroverzné, samostatná sekcia bola venovaná príprave nových odporúčaní pre parenterálnu a enterálnu výživu kriticky chorých pacientov.
Kľúčové slová: iatrogénny underfeeding, optimalizácia výživy, ICU-aquired weakness syndróm, gastrický reziduálny objem
Prevalencia iatrogénneho underfeedingu a optimalizácia výživy kriticky chorých pacientov
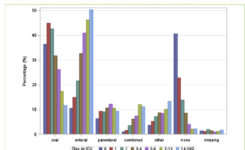
Prevalencia iatrogénneho underfeedingu u kriticky chorých pacientov je celosvetovo stále vysoká. Potvrdzujú to aj výsledky nedávno publikovanej prevalenčnej štúdie „Nutritition Day ICU“ (graf č. 1). Iniciácia nutričnej podpory je oneskorená, takmer nikdy nedosiahne denné odporúčané dávky energie a jednotlivých makronutrientov. Preskripcia výživy sa neriadi všeobecne platnými odporúčaniami, nezohľadňuje ani hmotnosť, ani celkový stav pacienta. Až 50 % pacientov v priebehu hospitalizácie na ICU pociťuje hlad, smäd a sucho v ústach. Enterálnu výživu na konci 1. týždňa hospitalizácie má sotva 50 % pacientov a parenterálnu výživu necelých 15 %. Vo všeobecnosti máme tendenciu nadmerne živiť pacientov s BMI < 18,5 a obéznych pacientov s BMI > 40 vystavujeme underfeedingu.(1) Výživa ICU pacientov má vplyv na rozvoj syndrómu svalovej slabosti kriticky chorých (ICU aquired weakness – ICUAW). Incidencia je vysoká, postihuje až 67 % pacientov na UPV trvajúcej dlhšie ako 10 dní. K rizikovým faktorom patrí ťažký priebeh sepsy, multiorgánové zlyhávanie (MOF), prolongovaná imobilizácia, hyperglykémia a vyšší vek pacientov. Úloha kortikosteroidov a myorelaxancií pri rozvoji ICUAW je stále nejasná. Prispieva k zvýšenej 1-ročnej mortalite a pri prepustení z nemocnice trpí týmto syndrómom stále 36 % pacientov. U časti pacientov sa vyvinie perzistujúci zápalový imunosupresívny katabolický syndróm. Kľúčovú úlohu v prevencii a liečbe zohráva agresívna liečba sepsy, optimálna inzulinoterapia, denné dodržiavanie sedačného okna a optimalizácia výživy kriticky chorých pacientov.(2) V katabolickej fáze treba redukovať denný prísun energie a bielkovín (počas 1. týždňa). Americká spoločnosť pre parenterálnu a enterálnu výživu vydala aktualizované odporúčania, na základe ktorých sa suplementárna parenterálna výživa pridáva až medzi 7. – 10. dňom. Výnimku tvoria ťažko malnutriční a vysokorizikoví pacienti s neadekvátnym enterálnym príjmom, u ktorých odporúča pridať suplementárnu parenterálnu výživu už v priebehu 1. týždňa. Energetický príjem by nemal presiahnuť 20 kcal/kg/deň s adekvátnou suplementáciou bielkovín ≥ 1,2 g/kg/deň. Európska spoločnosť pre klinickú výživu a metabolizmus má k suplementárnej parenterálnej výžive konzervatívnejší postoj. Odporúča začať parenterálnu výživu na 3. – 4. deň u ťažko malnutričných a potenciálne dlhodobo hospitalizovaných kriticky chorých pacientov.(8) V anabolickej fáze je nutné dodať pacientovi dennú odporúčanú dávku energie a jednotlivých makronutrientov, pričom dôraz sa kladie na suplementáciu bielkovín v maximálnej dennej odporúčanej dávke. Na zabudovanie bielkovín do svalov je dôležitá rehabilitácia. Nesmieme zabúdať na suplementáciu vitamínov a stopových prvkov, a to od 1. dňa preskripcie parenterálnej výživy.
Pri strate svalovej hmoty u kriticky chorých pacientov zohráva dôležitú úlohu glukagón. Jeho zvýšené hladiny prispievajú v pečeni k nadmernému katabolizmu bielkovín. Parenterálna suplementácia aminokyselín s cieľom prevencie úbytku svalovej hmoty nepotlačí katabolizmus bielkovín v pečeni navodený zvýšenou hladinou glukagónu. Rozbieha sa začarovaný kruh, keď zvýšený prísun bielkovín stimuluje zvýšenú produkciu glukagónu a ten v pečeni navodzuje zvýšený katabolizmus bielkovín.(5, 7)
V uplynulom období bolo publikovaných niekoľko metaanalýz, ktoré sa zaoberali optimalizáciou výživy u kriticky chorých pacientov. Porovnávali vplyv enterálnej a parenterálnej výživy na vznik infekčných komplikácií, skrátenie dĺžky trvania hospitalizácie na ICU, dĺžku trvania umelej ventilácie pľúc (UPV) a vplyv na mortalitu. Nižší verzus vyšší kalorický príjem u ICU pacientov nebol asociovaný s rozdielom v mortalite, rizikom vzniku pneumónie alebo dĺžkou trvania umelej pľúcnej ventilácie. Nižší kalorický príjem u pacientov živených enterálnou cestou bol spojený s redukciou infekčných komplikácií a skrátením dĺžky trvania hospitalizácie na ICU. Nárast infekčných komplikácií v skupine pacientov živených parenterálnou cestou bol vysvetlený vyšším kalorickým príjmom v porovnaní so skupinou pacientov, ktorí boli živení len enterálnou cestou.(3, 4)
Ďalšou diskutovanou témou na tohtoročnom ESPEN bol výber lipidových emulzií v parenterálnej výžive. Výsledky metaanalýzy recentne publikovanej v JPEN vyhodnotili dáta z 34 klinických štúdií. Vo väčšine štúdií nebol potvrdený priaznivý vplyv rybieho tuku na redukciu infekčných komplikácií, pokles mortality, dĺžky trvania nemocničnej ani ICU hospitalizácie a skrátenie času trvania UPV.(9) Vzhľadom na variabilitu a rozdielnu úroveň jednotlivých štúdií nie je doposiaľ možné priaznivý vplyv rybieho tuku ani potvrdiť, ani vyvrátiť.
Častým problémom, s ktorým sa o. i. stretávame v každodennej praxi, je dysfunkcia GIT. V marci 2017 boli publikované ESICM clinical practice guidelines, ktoré favorizujú včasnú enterálnu výživu. Výnimku tvoria pacienti s nekontrolovaným šokom, život ohrozujúcou hypoxémiou, hyperkapniou a acidózou, pacienti s črevnou ischémiou, akútnym krvácaním do GITu a pacienti s gastrickým reziduálnym objemom (GRV) > 500 ml/6 hod. Enterálna výživa je často prerušovaná zbytočne, dôležité je nevychádzať z jedného merania GRV. Zabránime tým ďalšiemu prehĺbeniu energetického deficitu kriticky chorých pacientov. Na viacerých pracoviskách majú zavedené protokoly na EV práve preto, aby sa zabránilo častému prerušovaniu EV. Neprítomnosť peristaltiky, obstipácia ani hnačka nie sú okamžité dôvody na zastavenie EV.(6)
Záver
Kriticky chorí pacienti sú vulnerabilní. Preskripcia enterálnej a parenterálnej výživy sa na väčšine pracovísk neriadi všeobecne platnými odporúčaniami, neprihliada na celkový stav ani na hmotnosť pacienta, ale riadi sa lokálnymi zvyklosťami. Treba si uvedomiť, čo potrebuje kriticky chorý pacient v akútnej a chronickej fáze. Výživa je súčasťou komplexnej starostlivosti a liečby, a preto by sme nemali zabúdať denne prepočítavať zloženie enterálnej a parenterálnej výživy. Preskripcia vitamínov a stopových prvkov je súčasťou parenterálnej výživy od 1. dňa.
MUDr. Jana Haščičová
OAIM, NOÚ, Bratislava
E-mail: jana.hascicova@nou.sk