Abstrakt
Tato práce uvádí kazuistiku pěti dospělých pacientů s rozsáhlým termickým poraněním, u nichž došlo ke ztrátě 30 % a více tělesných proteinů, kteří vyvinuli závislost na externím přívodu živin a u nichž jsme prokázali významnou mitochondriální dysfunkci v kosterním svalstvu. Tento stav byl úspěšně léčen pomocí kontinuální výživové podpory a s využitím rehabilitace iluzorními pohyby.
Klíčová slova: rozsáhlé popáleniny, hypermetabolismus, hyperkatabolismus, druhotná poranění, iluzorní pohyby, funkční proprioceptivní stimulace
Abstract
This paper presents a case report of 5 adult patients with an extensive thermal trauma who lost 30% or more of their body proteins, developed a dependence on external nutrient supply, and in whom we demonstrated significant mitochondrial dysfunction in the skeletal muscle. This condition has been successfully treated with continuous nutritional support and with the use of illusory movements rehabilitation.
Klíčová slova: large burns, hypermetabolism, hypercatabolism, secondary insults, illusory movements, functional proprioceptive stimulation
Úvod
Nemocní s rozsáhlým termickým traumatem jsou z řady důvodů vystaveni sekundárním inzultům, které udržují v chodu hyperinflamatorní stav a mohou vést k vyčerpání tělesných rezerv (1). Nejčastějšími druhotnými poškozeními jsou opakované chirurgické výkony provázené krevní ztrátou a prochladnutím, četné lokální a systémové infekce, orgánová selhání, dlouhodobá dysfunkce trávicího traktu a v neposlední řadě limitované možnosti fyzioterapie. Část nemocných je seniorního věku, se závažnými komorbiditami a s omezením pohybu již v předchorobí.
Rozsáhlé popáleniny vedou k metabolické dysfunkci. Dominující charakteristikou je u popálených hypermetabolický stav dosahující dlouhodobě 150–180 % klidového energetického výdeje (REE) pacienta (2). Přibližně 60 % tohoto navýšení REE je způsobeno ATP-dependentními procesy, jako jsou proteosyntéza nebo glukoneogeneze, 40 % jde na vrub tzv. prázdným cyklům a mitochondriální termogenezi (3). Druhou charakteristikou je výrazná inzulinová rezistence působící v inzulin-dependentních tkáních intracelulární nedostatek glukózy. Souběžná hyperinzulinemie ztěžuje, až zastavuje ketogenezi v játrech; volné mastné kyseliny jsou v cytosolu buněk resyntetizovány zpět na triacylglyceroly v ATP konzumujících cyklech (4), a nejsou tak plně využity jako energetický substrát. Energetickým zdrojem pro některé tkáně (zvláště kosterní svalstvo) tak zůstávají pouze vlastní aminokyseliny (AMK). Svaly také ve velkém uvolňují do krve některé AMK pro potřeby glukoneogeneze a pro syntézu proteinů akutní fáze. To vede u popálených k rozsáhlé devastaci svalstva. Přítomnost prozánětlivých cytokinů a kortizolu inhibuje účinky proteoanabolických hormonů, rozvíjí se anabolická rezistence svalu. Popálený pacient ztrácí denně stovky gramů svalové hmoty (až 1 kg/den). Stav není reverzibilní zevním dodáním energetických substrátů (5). To rezultuje v život ohrožující sarkopenii. Ztráta 30 % hmotnosti myokardu způsobí srdeční selhávání, atrofie bránice a dýchacích svalů prodlužuje dechovou nedostatečnost a závislost na ventilátoru. Kumulativní ztráta 25 % a více tělesných proteinů je provázena orgánovým selháváním (6). Mnohdy tak je, navzdory adekvátní léčebné výživě, uzavřen bludný kruh: orgánové dysfunkce (jaterní a renální nedostatečnost) jsou spolu s metabolickými změnami (inzulinová rezistence, anabolická rezistence svalu) příčinou negativní proteinové bilance, která dále zhoršuje funkci orgánů a prohlubuje svalový katabolismus. Tento stav byl pro svou vysokou mortalitu některými autory nazván dusíková smrt (7).
Aktivní pohyb je silným anabolickým stimulem kosterního svalu, který by mohl rozetnout circulus vitiosus svalové autofágie. Práce svalu vede k nitrobuněčné i systémové signalizaci, jejímiž důsledky jsou snížená proteolýza, svalový růst, syntéza svalového glykogenu a zlepšení lokálního prokrvení. Na systémové úrovni se tato změna myocytárního metabolismu projevuje poklesem inzulinové rezistence, zvýšenou glukózovou clearance a pozitivní dusíkovou bilancí (8). Možnosti aktivního i pasivního pohybu jsou ale u rozsáhle popálených (a nejen u nich) velmi omezené.
Jako alternativa se u těch, kteří nemohou být standardně rehabilitováni, nabízí fyzioterapie pomocí proprioceptivní neuromuskulární facilitace (PNF), tzv. iluzorních pohybů, kdy k žádnému reálnému pohybu nedochází. Jedná se o relativně novou léčebnou techniku, která se používá převážně u nemocných po iktu, a to kvůli prokázanému neurotropnímu efektu. Stimulací hluboké propriocepce pomocí vibrací na končetinách se navozuje vjem pohybu dané končetiny v příslušných korových centrech mozku, která pak vysílají nervové podněty směrem ke končetině (9, 10, 11). Navíc stimulace jedné svalové skupiny (flexorů) pomocí spinálního reflexu vede k reflexnímu napětí antagonistů (extenzorů). Pacienti při vědomí tak mají iluzi pohybu stimulovaných končetin, a to podle navoleného typu pohybu (chůze, běh, dřepy, jízda na kole, mávání pažemi apod.), aniž by se sebeméně pohnuli. Nedochází přitom k ovlivnění vitálních funkcí nemocného a vibrace nejsou bolestivé. Vibrační jednotky se mohou (bez snížení funkčnosti) přikládat na předdefinované stimulační lokality i přes obvazový materiál (12). Nabízí se tak jejich využití u kriticky nemocných s limitovanými možnostmi fyzioterapie (kromě popálených ještě např. u pacientů na ECMO, v pronační poloze, po rozsáhlých operacích nebo traumatech) nebo u polyneuromyopatií kriticky nemocných (13). Podle našeho nejlepšího vědomí však dosud nebyly žádné práce o využití PNF v intenzivní péči publikovány.
Soubor nemocných
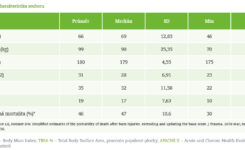
Kazuistický soubor tvoří pět rozsáhle popálených mužů léčených na Klinice popáleninové medicíny 3. lékařské fakulty Univerzity Karlovy a Fakultní nemocnice Královské Vinohrady (KPM) v době od 1. ledna 2019 do 31. srpna 2020, u nichž došlo ke ztrátě více než 25 % tělesné hmotnosti a hibernačním symptomům. Jejich příjmová charakteristika je zanesena v tabulce č. 1.
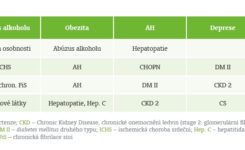
V tabulce č. 2 jsou uvedeny příjmové komorbidity. Příčinou úrazu byl u dvou nemocných suicidiální pokus (upálení), u dvou nehoda při potencování hoření a jeden byl poraněn výbuchem při přípravě drog.
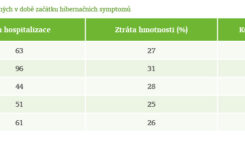
Průměrná délka hospitalizace byla 146 dnů, s mediánem 90 dnů. Průběh léčby byl u všech těchto pacientů komplikován poruchou lokálního hojení ran, poruchou hojení odběrových ploch, odlučováním kožních štěpů, opakovanými lokálními a systémovými infekcemi a poruchou střevní pasáže. Dva pacienti byli dialyzováni, u tří se rozvinula klinicky významná hepatopatie s ikterem. Dva nemocní byli postiženi klostridiovou enterokolitidou. Dalšími komplikacemi byly u jednotlivých osob: septický šok, krvácení do GIT, ARDS, pneumonie, srdeční zástava s úspěšnou resuscitací a polyneuropatie kriticky nemocných.
Všichni pacienti byli při příjmu a po dobu několika týdnů ventilováni a sedováni. Po přijetí byla těmto pěti zraněným zavedena nazoduodenální sonda a během prvních 24 hodin byla zahájena enterální výživa kontinuálním podáváním oligomerního přípravku. Nutriční terapie byla ordinována na podkladě denního měření REE indirektní kalorimetrií (Q-NRG+, Cosmed, Italy) a dusíkové bilance, s cílem dosažení vyrovnaných bilancí od 10. dne po přijetí. Vyrovnané kalorické bilance (s příjmem 35–45 kcal/kg ideální tělesné hmotnosti, IBW) se dařilo kombinací enterální a parenterální výživy dosáhnout, byť mnohdy za cenu intenzifikované terapie i.v. inzulinem (v průměru 36 j/den, s rozptylem 0–288 j/den). Dusíková bilance však zůstávala dlouhodobě negativní, v průměru –8 (0 až –24,4) g/den. Zvýšený přísun aminokyselin vedl ke zvýšené produkci urey, se stoupajícími odpady urey do moči nebo s narůstající uremií, zatímco viscerální proteiny zůstávaly nízké: celková bílkovina pod 50 (36–49) g/l, albumin pod 25 (11–24) g/l, prealbuminu pod 0,1 (0,01–0,1) g/l a transferinu pod 2 (0,7–1,5) g/l (hladiny retinol-binding proteinu a aktivitu cholinesterázy jsme neměřili).
Pravidelně jsme monitorovali hladiny stopových prvků (Fe, P, Zn, Se, Cu, Mg) a vitaminů (A, D, E, C, B1, B2, B12) s jejich případnou suplementací nad rámec standardní preskripce. Hladiny hormonů štítné žlázy a kortizolu se pohybovaly při dolní hranici fyziologických mezí. V indikovaných případech jsme provedli synactenový test, opět s fyziologickými výsledky při dolní hranici normy.
Markery zánětu (počet bílých krvinek, Intensive Care Infection Score, prokalcitonin a C-reaktivní protein) se průběžně měnily dle klinické situace konkrétního pacienta, nevybočovaly však z mezí, jaké jsou vídány u rozsáhle popálených.
Nemocné jsme pravidelně vážili, ale kvantifikovat klinicky zjevnou sarkopenii jsme vzhledem ke specifitě rozsáhle popálených nedokázali; ač jsme zvažovali existující zobrazovací metody vyšetření svalové hmoty, narazili jsme na technické, medicínské nebo etické problémy.
U všech těchto nemocných byla primárně přítomna porucha hojení. Popálené plochy se nehojily, infikovaly se, vyžadovaly opakované chirurgické intervence. Kožní štěpy se odhojovaly (a to i po případném primárním přihojení), odběrové plochy se hojily sekundárně.
Druhým příznakem byla postupná ztráta adaptivní reakce na hladovění. Při přerušení umělé výživy začali být tito nemocní spaví, apatičtí, přestávali komunikovat, klesala jim tělesná teplota, spontánní pohybová aktivita se snížila na minimum. Naopak po restartu umělé výživy se jejich kondice vracela do původního stavu. V analogii s přenosnou elektronikou jsme těmto hibernačním symptomům začali na našem pracovišti říkat „syndrom slabé baterie“. Docházelo k tomu převážně v perioperačním období, kdy byla nutrice přerušena z indikace celkové anestezie a operace. Měření indirektní kalorimetrií u všech pěti nemocných prokázalo pokles BMR pod 80 % proti příslušnému odhadu (dle Harrise a Benedicta). Měření REE ale bylo při přívodu stravy v souladu s předpokládaným energetickým výdejem.
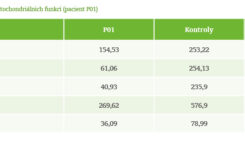
Třetím společným znakem byla přítomnost významné mitochondriální dysfunkce kosterních svalů. Analýzou mitochondriální respirace (Oxygraph-2k, Oroboros Instruments Corp, Austria) ze svalových biopsií jsme prokázali sníženou produkci ATP a sníženou činnost komplexů dýchacího řetězce ve srovnání s kontrolami uzdravených pacientů (tabulka č. 4).
Léčebné intervence
Pacienty jsme zařadili do režimu kontinuálního přívodu živin, tedy bez nočních pauz a bez přerušení výživy v perioperačním období. Kalorický příjem byl adjustován na základě denního měření REE, s cílem 10% navýšení nad aktuální hodnotu REE. Enterálně byla podávána polymerní výživa. Doplňková parenterální výživa byla ordinována ve formě tříkomorových komerčních vaků. Pokud byl pacient schopen jíst, byla mu předepsána vhodná dieta. Dodávky proteinů nad 1,5 g / kg / 24 h byly ordinovány podle momentální tolerance aminokyselin, s cílem dosáhnout přívodu 3 g / kg / 24 h (15). Perioperačně se podávala parenterální výživa a u nemocných s jejunální sondou i výživa enterální. 1× týdně jsme přerušili veškerou výživu na 8 hodin, nemocného vyšetřili na přítomnost hibernačních symptomů a změřili BMR indirektní kalorimetrií.
U nemocných jsme také nad rámec možné (zpravidla pasivní) fyzioterapie zahájili rehabilitaci formou iluzorních pohybů (Vibramoov, Mane, France). U každého z pacientů byla ordinována 30minutová seance střední intenzity dvakrát denně, kterou prováděl fyzioterapeut nebo zaškolený personál. V průběhu cvičení jsme kromě vitálních funkcí měřili i REE před a po cvičení.
Výsledky
Normalizace BMR definované jako dosažení 100% hodnoty vypočítané dle rovnice Harrise a Benedicta se podařilo dosáhnout po třech až čtyřech týdnech léčebných intervencí.
Rehabilitace iluzorními pohyby měla tyto metabolické efekty:
– Po cvičení byl respirační kvocient (RQ) v průměru o 4 % nižší než před cvičením, a to signifikantně (p = 0,002). Snížilo se VO2 i VCO2, ale VO2 více. Změna REE byla nesignifikantní;
– změnila se utilizace jednotlivých substrátů: klesla utilizace sacharidů (p = 0,001) a proteinů (p = 0,028), zvýšila se utilizace tuků (p = 0,001);
– v průměru od čtvrtého dne cvičení se začala snižovat denní ztráta dusíku a v průměru od osmého dne se bilance dusíku vyrovnala. Pozitivní dusíkové bilance bylo dosaženo v průměru po dvou týdnech cvičení.
U žádného pacienta jsme nezaznamenali změnu ve vitálních funkcích ani žádné komplikace. Jeden pacient považoval za nepříjemný (ale snesitelný) tlak vibračních čidel v oblasti Achillových šlach. Jeden pacient preferoval program jízdy na kole před ostatními (do jisté míry volitelnými) iluzemi.
U všech pacientů došlo ke zlepšení klinického stavu, popálené i odběrové plochy se dohojily a všichni nemocní byli propuštěni z JIP a potom i z nemocnice, žádný nezemřel.
Diskuze
Na JIP KPM bylo v daném období přijato 186 pacientů, z toho 51 pacientů s popáleninami na 20 a více % TBSA. U 5 z nich (2,7 % z celku a 9,8 % z rozsáhle popálených) došlo navzdory snaze o adekvátní výživu k rozvoji závažné malnutrice spojené s extrémní ztrátou tělesných proteinů a následné poruše adaptační reakce na hladovění. Klinickým příznakem u daných pacientů byly projevy hibernace během lačnění a odeznění stavu, když lačnění skončilo. Nazvali jsme tyto projevy „syndromem slabé baterie“. Stupeň poruchy koreloval s BMR, tedy výraznější symptomy byly patrny u pacientů s velmi nízkým BMR.
Charakteristickým rysem byla i mitochondriální dysfunkce kosterního svalstva, která mohla být příčinou i důsledkem tohoto syndromu (16). Funkce mitochondrií a bioenergetická dysfunkce u kriticky nemocných jsou předmětem našeho současného výzkumu.
Léčebným opatřením byla kontinuální, mírně hyperkalorická výživa. Domníváme se, že takto extrémní metabolická dysfunkce, metabolické selhání tohoto stupně, vyžaduje změnu paradigmatu v podávání výživy, tj. její kontinuální podávání bez (nočních a perioperačních) pauz, a to až do doby, než se normalizuje metabolická odpověď na hladovění.
Ve snaze o překonání anabolické rezistence svalu jsme u nemocných zahájili rehabilitaci pomocí iluzorních pohybů. Jejich použití mělo bezprostřední i dlouhodobé metabolické účinky. Pro nás byl překvapivý signifikantní pokles RQ a zvýšená utilizace tuků během cvičení a po cvičení, protože pacient se při použití PNF vůbec nepohybuje a veškerý „pohyb“ se odehrává jen v jeho mozku, a to prokazatelně i u hluboce sedovaných pacientů (12). Pro tento jev nemáme vysvětlení a je předmětem našeho recentního výzkumu. Dlouhodobým účinkem bylo navození pozitivní dusíkové bilance a zlepšené hojení ran, jistě i v součinnosti s podávanou nutricí.
Závěr
Navzdory možnostem, které v současné době máme na poli léčebné výživy a monitoringu nutričního stavu, stále existují pacienti ohrožení extrémním proteinovým katabolismem. Naše kazuistika ukazuje, že tato situace je reverzibilní, pokud je tato porucha diagnostikována a jsou použity individualizované léčebné postupy nutriční podpory a fyzioterapie. Rehabilitace pomocí iluzorních pohybů se zdá být vhodnou, bezpečnou a účinnou metodou u pacientů s limitovanou možností jiných druhů pohybové podpory.
MUDr. Bohumil Bakalář
Klinika anesteziologie a resuscitace 3. lékařské fakulty
Karlovy Univerzity a Fakultní nemocnice Královské Vinohrady, Praha
e-mail: bohumil.bakalar@lf3.cuni.cz
prof. MUDr. Marcela Grünerová-Lippertová, Ph.D.
Klinika rehabilitačního lékařství 3. lékařské fakulty
Karlovy Univerzity a Fakultní nemocnice Královské Vinohrady, Praha